Groupe 2
Déterminants cellulaires de la neuroprotection
Parmi les déterminants cellulaires des processus neurodégénératifs observés dans toutes les maladies neurodégénératives, le dysfonctionnement mitochondrial, le stress du réticulum endoplasmique (RE) et l’altération de la communication RE-mitochondrie sont apparus comme des évênements communs responsables de la persistence de la toxicité. Les interactions entre RE et mitochondries sont altérées dans toutes les pathologies neurodégénératives et de nombreuses maladies génétiques. La question du rôle des domaines d’interaction hautement fonctionnalisés entre RE et mitochondries, connus sous le nom de MAM, est actuellement un très étudiée. Les MAM sont stabilisées par des ponts protéiques et séquestrent de nombreux assemblages protéiques, où les échanges focaux de Ca2+ sont permis par les complexes IP3 sur le RE et VDAC1/MCU sur les membranes mitochondriales. Dans la maladie d’Alzheimer (MA), par exemple, les présénilines sont exprimées dans les MAM et la toxicité Aβ affecte les contacts RE-mitochondries. La protéine Tau associée aux microtubules modifiés a un impact sur le stress du RE et la réponse UPR qui semble dépendre de la mutation et/ou du statut oligomèrique.
Nous avons précédemment montré que les agonistes activant le récepteur sigma-1 (S1R), une protéine hautement concentrée dans les MAM, permettaient une neuroprotection efficace dans des modèles animaux de MA ou de sclérose latérale amyotrophique (SLA). S’appuyant sur une expertise en neuropharmacologie, en génétique moléculaire et en biologie cellulaire, notre équipe développe un projet global ciblant ces déterminants cellulaires de la neurodégénérescence avec un accent particulier sur le S1R en tant que (1) chaperon prototype permettant la restauration fonctionnelle de la communication RE-mitochondrie et (2) plate-forme cible pour le développement de candidats médicaments innovants, à la suite de la Blarcamesine ou de la Pridopidine, développés dans la MA, la maladie de Huntington et la SLA.
La stratégie de l’équipe, résumée dans le schéma suivant, est développée en 4 axes complémentaires.
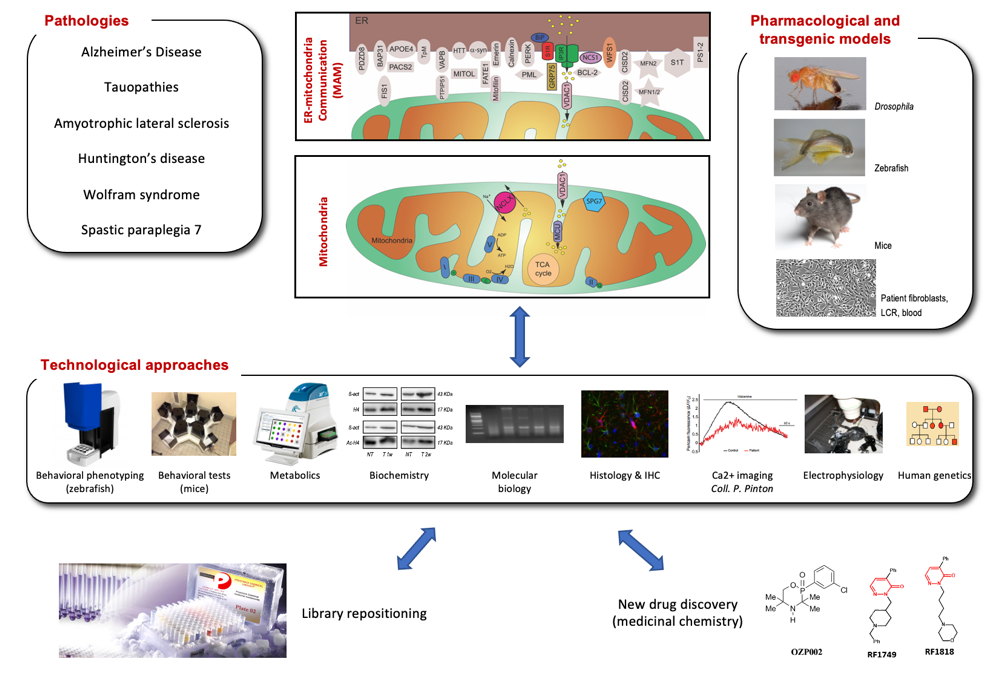
Projet 1. Déficit de communication entre RE et mitochondries dans les maladies neurodégénératives (leader du groupe : Benjamin Delprat)
Projet 2. Lutte contre les dysfonctionnements mitochondriaux dans les maladies neurodégénératives (leader du groupe : Jean-Charles Liévens)
Projet 3: Réponse au stress des ER physiopathologiques dans les tauopathies (leader du groupe : Mireille Rossel)
Projet 4: Programmes de développement pharmacologique : agonistes S1R, FENM et au-delà (leader du groupe : Tangui Maurice)